Dans le numéro précédent, nous avons partagé l'étude sur l'utilisation du D ()-tréhalose dihydraté dans la cryoconservation des cellules précurseurs d'oligodendrocytes humains (OPC). L'étude a conclu que le milieu de cryoconservation ajouté avec du D ()-tréhalose dihydraté était adapté à la cryoconservation à long terme des OPC et a contribué à améliorer le taux de récupération cellulaire.
Dans ce numéro, examinons l'étude du cryoprotecteur (CPA) du D ()-tréhalose dihydraté glycérol dans la cryoconservation de cellules souches dérivées d'adipeux (ADSC) pour favoriser la cicatrisation des plaies.
Étude du CPA du D ()-tréhalose dihydraté glycérol dans la cryoconservation des ADSC pour la promotion de la guérison des plaies
Les cellules souches dérivées de l'adipeux (ADSC) ont le potentiel de se différencier en cellules d'origine mésodermique, telles que les cellules adipogéniques, ostéogéniques et chondrogéniques, et ont également des effets immunosuppresseurs, qui ont des perspectives d'application clinique en médecine régénérative et dans le traitement des troubles immunitaires réfractaires. La recherche ADSC est devenue l'un des domaines de recherche les plus chauds de la communauté médicale.
L'un des problèmes de la thérapie ADSC actuelle est la cryoconservation efficace et sûre des ADSC. Le CPA traditionnel est 10% DMSO 90% FBS. Cependant, l'utilisation du DMSO dans la cryoconservation à long terme des cellules peut augmenter le taux d'apoptose car le DMSO est cytotoxique et perturbe le processus de méthylation de l'ADN des tissus, tandis que le FBS contient des protéines xénogéniques d'origine animale qui peuvent introduire des virus zoonotiques ou entraîner des réactions allergiques. Par conséquent, ce CPA ne convient pas pour une utilisation clinique.
Des chercheurs du neuvième hôpital du peuple affiliés à l'école de médecine de l'Université Jiao Tong de Shanghai ont trouvé dans leIn vitroExpérimenter que le CPA composite de 1.0 mol/L D ()-tréhalose dihydraté 20% glycérol n'a montré aucune différence statistique dans la viabilité cellulaire, capacité de prolifération cellulaire lorsqu'elle est utilisée pour la cryoconservation des ADSC par rapport au CPA traditionnel, mais la capacité de migration était nettement meilleure.
Les chercheurs ont exploré plus en détail leIn vivoEffets biologiques des ADSC post-dégel cryoconservés dans le CPA composite ci-dessus dans les modèles enroulés par souris.
① CPA composite (groupe d'essai): 1.0 mol/L D ()-tréhalose dihydraté + glycérol 20%, avec le solvant d'une solution saline tamponnée au phosphate (PBS, pH 7.4).
② CPA traditionnel (groupe témoin 1): 10% DMSO 90% FBS.
③ Une solution saline normale (groupe témoin 2): sans cryoprotection.
Les CPA ont été préparés avant utilisation et filtrés à travers un filtre de 0.22 μm.
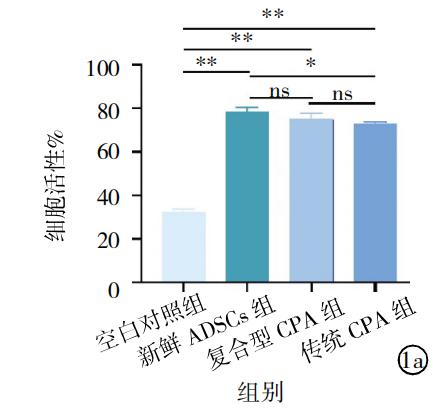
① Viabilité et morphologie des cellules:
Les cellules souches dérivées de l'adipeux (ADSC) cryopréservées avec le CPA composite ont maintenu une bonne viabilité cellulaire et une bonne morphologie après la décongélation. Il n'y avait pas de différence significative dans la viabilité cellulaire entre le groupe d'essai, le groupe témoin 1 et le groupe ADSC frais. La morphologie cellulaire des ADSC des trois groupes ci-dessus est restée fondamentalement la même après avoir été cultivée dans l'incubateur pendant 72 h.

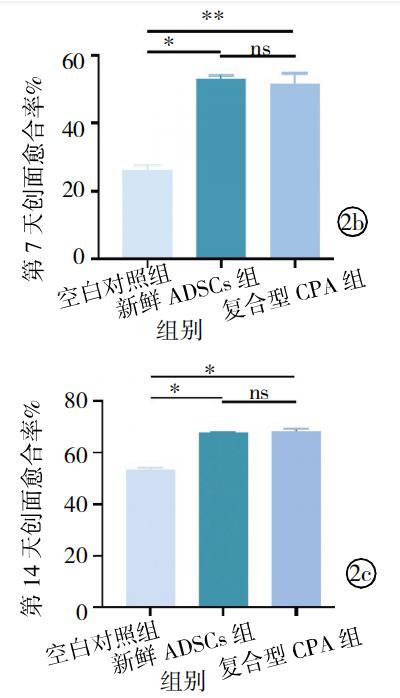
② Taux de guérison de la plaie:
Dans la plaie des modèles enroulés par souris, des ADSC cryoconservés avec le CPA composite, des ADSC frais et une solution saline normale ont été injectés respectivement.
Le 7e jour, le taux de cicatrisation des plaies pour le CPA composite était significativement plus élevé par rapport au groupe témoin 2, et il n'y avait pas de différence significative par rapport au groupe ADSC frais.
Au 14e jour, la cicatrisation des plaies des trois groupes a suivi la même tendance.
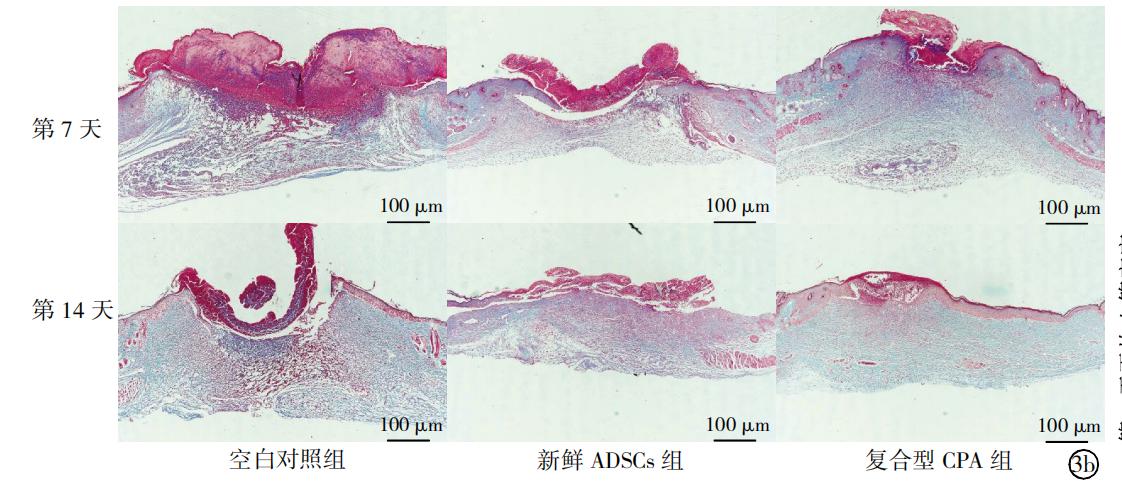
③ Effet sur la réépithélialisation de la plaie et le dépôt de collagène
Le 14e jour, la réépithélialisation de la plaie était meilleure pour le groupe test et le groupe ADSC frais, pour lesquels le tissu de granulation était formé et le collagène était uniformément et ordonné distribué. Les résultats ont indiqué que les ADSC cryoconservés avec le CPA composite ont des fonctions biologiques de promotion de la réépithélialisation des plaies et du dépôt de collagène similaires aux ADSC frais.
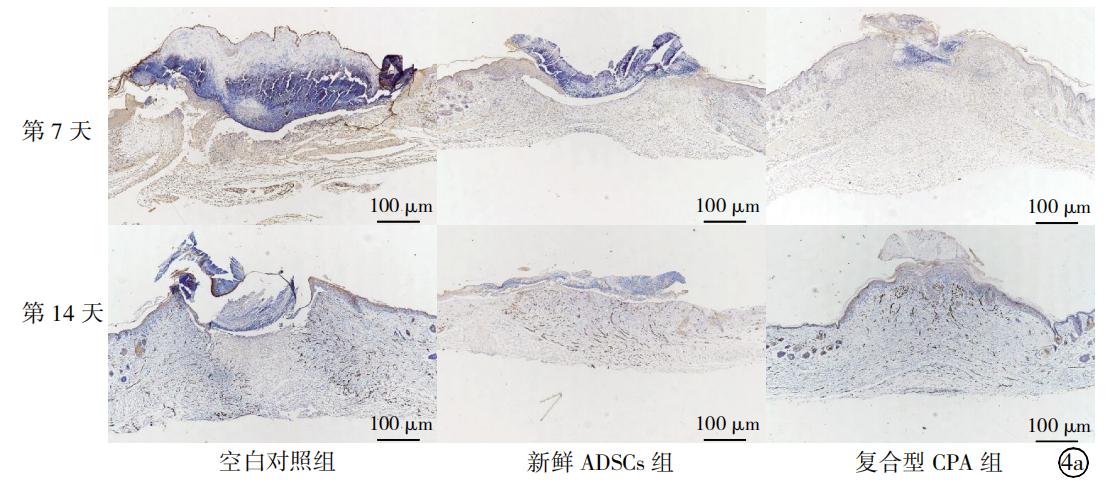
④ Effet sur la capacité de l'angiogenèse
Le CD31, également connu sous le nom de molécule d'adhésion plaquette-endothéliale, est principalement utilisé pour démontrer la présence de cellules endothéliales et évaluer l'angiogenèse. La coloration par immunofluorescence du CD31 est généralement effectuée pour observer l'angiogenèse dans les tissus infectés pendant le traitement.
Les 7e et 14e jours, une coloration par immunofluorescence du CD31 a été réalisée sur le tissu de la plaie et des données quantitatives ont été recueillies. Les résultats ont montré que les deux ADSC cryoconservés avec le CPA composite et les ADSC frais pourraient effectivement promouvoir l'angiogenèse.
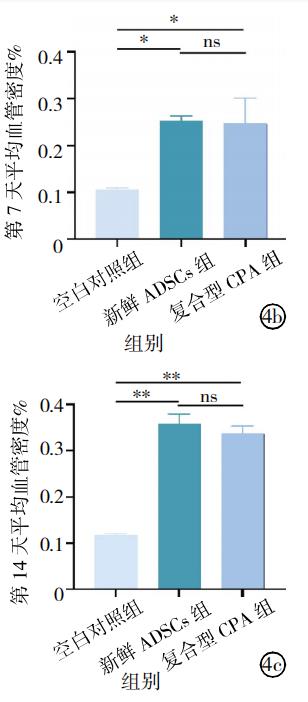
La cicatrisation des plaies est un processus pathologique dynamique et complexe impliquant la coordination mutuelle entre les cellules, les facteurs de croissance, la matrice extracellulaire, les nerfs, ainsi que les vaisseaux sanguins.
Les cellules souches dérivées de l'adipeux (ADSC) sont un type de cellules souches mésenchymateuses adultes, qui peuvent favoriser le dépôt de collagène, la vascularisation des tissus par la paracrine de diverses cytokines, et participer à la régulation immunitaire pour favoriser la cicatrisation des plaies. De plus, les ADSC peuvent se différencier en cellules épithéliales, kératinocytes et fibroblastes dermiques, qui favorisent directement la cicatrisation des plaies.
Les ADSC sont généralement obtenus par des interventions chirurgicales. Le potentiel de différenciation multilignée des ADSC diminue considérablement avec l'augmentation de l'âge des donneurs. Si les ADSC obtenus d'un jeune donneur au moyen d'une seule opération peuvent être cryoconservés, puis utilisés plusieurs fois au besoin, le coût du traitement des patients peut être considérablement réduit, et l'impact de l'âge des donneurs sur les résultats du traitement peut être réduit.
Dans cette étude, des modèles de plaies dorsales de souris ont été utilisés pour comparer les effets thérapeutiques des ADSC cryoconservés après décongélation et des ADSC frais. Selon les résultats, les ADSC cryoconservés avec le CPA composite ont montré la même capacité à favoriser la cicatrisation des plaies que les ADSC frais après décongélation. L'utilisation du cryoprotecteur composite de 1.0 mol/L D ()-tréhalose dihydraté 20% glycérol pour la cryoconservation des ADSC n'a pas affecté leIn vivoFonction biologique des cellules.
Les cryoprotecteurs composites peuvent exercer des effets protecteurs complémentaires lors de la congélation cellulaire par différents mécanismes.
Le D ()-dihydrate de tréhalose, en tant que cryoprotecteur non perméable, a un poids moléculaire relativement faible et forme une membrane protectrice sur la surface cellulaire, réduisant la cryo-lésion des cellules. Cependant, le D ()-tréhalose dihydraté ne peut pas pénétrer dans la membrane cellulaire, ce qui limite son efficacité protectrice.
Le glycérol, en tant que cryoprotecteur perméable, joue un rôle protecteur en augmentant la viscosité de la solution et en réduisant la formation de cristaux de glace, et peut aider D(+)-le tréhalose dihydraté pénètre dans la membrane cellulaire pour améliorer l'effet protecteur du D ()-tréhalose dihydraté.
Cette étude a montré que le CPA composite sûr et non toxique du D ()-tréhalose dihydraté glycérol pourrait protéger efficacement la viabilité et les fonctions biologiques des ADSC pendant la congélation, et s'assurer que les cellules ont le même effet de favoriser la régénération des tissus que les ADSC frais après décongélation. C'est un cryoprotecteur de cellules souches biologiquement sûr avec de grandes perspectives d'application clinique.